|
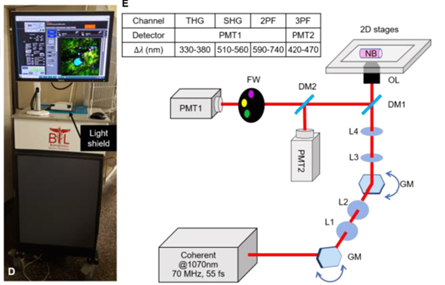
组织病理学切片一直是癌症临床评估手术标本和做出诊断决定的金标准,然而,常规组织学检查需要对进行组织固定、切片、染色等工序,耗时耗力。为了加快癌症诊断的过程,各种光学成像技术正越来越广泛地应用于临床及术中,通过实时的组织学监测提供重要的诊断和预后信息。目前大多数术中光学成像是基于荧光染料,不仅会破坏样本本身的微环境,还会改变组织内源性光学特征。本期介绍集成化无标记多模态非线性成像系统,可以用于检测乳腺癌。 图1为该成像系统的示意图, 光源为商用的紧凑型光纤激光器,重频为70MHz,脉宽约为55fs,系统集成了双光子荧光(2PEF)、三光子荧光(3PEF)、二倍频(SHG)和三倍频(THG)四个成像模态,其中信号较弱的3PEF信号单独收集,其余三通道信号由另一个PMT通过电动波轮切换连续收集,整体集成在一个便携推车中(35”W × 35”L × 45”H)。
图1 成像系统示意图 [1] 为了测试系统在光学组织评估中的表现,研究人员进行了术中切除的人类乳腺样本的成像,成像结果见图2:图A中SHG信号展示了胶原纤维沿红色虚线方向有序排列,图B和C的红色箭头分别指示了血管和乳腺导管及脂肪细胞,图D为未发生病变乳腺样本成像结果,可见未病变样本胶原纤维呈卷曲致密状,而癌变组织中,肿瘤细胞会沿排列有序的胶原纤维发生浸润。
图2 人类乳腺样本成像结果 [1] 除胶原纤维排布方式外,癌症诊断还可以借助该系统对肿瘤微环境中细胞外囊泡(EV)的空间分布的成像。实验中发现THG信号与EV分析高度相关,如图3所示:图A-C三幅图是多模态成像,图D-F是对应的H&E染色成像,图G-I是由THG图像处理得到的二值图,可以清晰地得到EV的分布。第一排展示了一个EV的富集区域,第二排是粘连早期时的EV 分布,基本分布在胶原纤维区域之外,其中红色区域是肿瘤与胶原纤维区域的边界,最后一排是粘连后期,已经发生了癌细胞浸润,此时在胶原纤维中EV的分布密度明显增加。
图3 肿瘤微环境中的EV空间分布成像 [1] 此外还可以获得EV的代谢信息,无标记成像中一般采用已建立的氧化还原比定义:FAD/(FAD+NAD(P)H),计算中为信号强度比:2PF/(2PF+3PF)。图4为手术中新鲜切除的正常和癌症人类乳腺组织的代表性无标签图像,下方为不同癌症分期(正常、1期至3期)患者的EV代谢谱。晚期癌症患者的EV代谢谱形似高斯分布,平均氧化还原比值较低,这是由于癌细胞中富含NAD(P) H,代谢活性更高。
图4 EV代谢谱分析 [1] 以上诊断参数结合AI及深度学习,可以对癌变倾向分级实现自动化定量癌细胞检测、分类和诊断,见图5。
图5 AI/DL癌症分析示意图 [1] 研究人员在实验中采用犬类动物手术样本测试了系统对活检组织的可行性(见图6),活检组织也可以获得与切片样本同样良好的成像效果。
图6 活检样本成像结果 [1] 总体来说,该集成的多模态显微镜系统可以对术中活检样本进行光学评估,有望成为辅助癌症诊断的强有力工具。 参考文献: [1] Yang L, Park J, Marjanovic M, et al. Intraoperative label-free multimodal nonlinear optical imaging for point-of-procedure cancer diagnostics[J]. IEEE Journal of Selected Topics in Quantum Electronics, 2021, 27(4): 1-12. |








 收藏
收藏 打印
打印